Prawo farmaceutyczne - jakie zmiany?
2015-03-17 10:25
![Prawo farmaceutyczne - jakie zmiany? [© Andrzej Tokarski - Fotolia.com] Prawo farmaceutyczne - jakie zmiany?](https://s3.egospodarka.pl/grafika2/prawo-farmaceutyczne/Prawo-farmaceutyczne-jakie-zmiany-153092-200x133crop.jpg)
Zmiany w prawie farmaceutycznym © Andrzej Tokarski - Fotolia.com
Przeczytaj także: Kontrowersyjne prawo farmaceutyczne. Spór o 1%
Na podstawie nowelizacji wprowadzono definicję sfałszowanego produktu leczniczego, która ma pozwolić na odróżnienie tego rodzaju produktu od innych nielegalnych produktów leczniczych, a także definicję sfałszowanej substancji czynnej. Sfałszowany produkt leczniczy oraz sfałszowana substancja czynna zostały przy tym objęte procedurami zmierzającymi do wyeliminowania takich produktów i substancji z obrotu. Jednocześnie wprowadzono nowe środki służące realizacji powyższego celu. Jednym z nich jest nowy mechanizm ostrzegania przez Głównego Inspektora Farmaceutycznego podmiotów uprawnionych do obrotu produktami leczniczymi oraz państw członkowskich Unii Europejskiej lub państw członkowskich EFTA - stron umowy o Europejskim Obszarze Gospodarczym, o uzasadnionym podejrzenia wady jakościowej lub sfałszowania produktu leczniczego stanowiących poważne zagrożenie dla zdrowia publicznego. Dodatkowo przewidziano, że w razie uznania, że ww. produkt leczniczy został już wydany pacjentom, Główny Inspektor Farmaceutyczny w terminie 24 godzin wydaje obwieszczenie w celu poinformowania o możliwości zwrotu tego produktu do aptek. W nowelizacji zawarto także regulacje karne dotyczące fałszowania produktów leczniczych.W drodze nowelizacji zmodyfikowano przepisy dotyczące zezwoleń na wytwarzanie produktów leczniczych oraz zezwoleń na import produktów leczniczych. Obowiązujące dotychczas odrębne regulacje dotyczące wydawania ww. zezwoleń zostały bowiem zastąpione przez jedną ujednoliconą procedurę regulującą ich wydawanie.
Do zmienionej ustawy dodano także nowy rozdział poświęcony wytwarzaniu, importowi i dystrybucji substancji czynnej, w którym wskazano, że podjęcie działalności w ww. zakresie wymaga uzyskania wpisu do Krajowego Rejestru Wytwórców, Importerów oraz Dystrybutorów Substancji Czynnych. Organem właściwym do dokonania, odmowy dokonania lub zmiany wpisu, a także wykreślenia podmiotu z ww. rejestru uczyniono Głównego Inspektora Farmaceutycznego. Na importerów substancji czynnej nałożono także nowe obowiązki. Jednym z nich jest obowiązek związany z wprowadzeniem instytucji pisemnego potwierdzenia wystawianego przez właściwy organ kraju trzeciego w momencie eksportu substancji czynnej do państwa członkowskiego Unii Europejskiej lub państwa członkowskiego EFTA, strony umowy o Europejskim Obszarze Gospodarczym.
fot. Andrzej Tokarski - Fotolia.com
Zmiany w prawie farmaceutycznym
Do najistotniejszych zmian należą m.in. nowe przepisy dotyczące sfałszowanego produktu leczniczego, zmiany w zakresie wytwarzania, importu, dystrybucji hurtowej oraz sprzedaży wysyłkowej produktów leczniczych, a także zmiany odnośnie wytwarzania, importu i dystrybucji substancji czynnych.
Obowiązek ten polega na imporcie wyłącznie tej substancji czynnej, w stosunku do której dołączono ww. pisemne potwierdzenie. Dokument ten powinien przy tym zawierać określone informacje, w tym m.in. potwierdzenie, że zasady Dobrej Praktyki Wytwarzania stosowane przez wytwórcę substancji czynnej przeznaczonej na eksport są zgodne z wymaganiami Dobrej Praktyki Wytwarzania określonej w polskich przepisach oraz, że dany wytwórca substancji czynnej podlega regularnej inspekcji. Nowelizacja określiła także zasady przeprowadzania inspekcji u polskich wytwórców substancji czynnych, które, zgodnie z nowymi przepisami, mają odbywać się z częstotliwością ustalaną w oparciu o analizę ryzyka przeprowadzaną przez inspektorów do spraw wytwarzania Głównego Inspektoratu Farmaceutycznego.
Nowelizacja wprowadziła do zmienianej ustawy także nowy rozdział dotyczący pośrednictwa w obrocie produktami leczniczymi, z wyłączeniem pośrednictwa w obrocie produktami leczniczymi weterynaryjnymi. W rozdziale tym określono, jakiego rodzaju działalność stanowi pośrednictwo w obrocie produktami leczniczymi oraz określono jakie wymagania należy spełnić celem prowadzenia tego rodzaju działalności. Jak wynika z ww. regulacji pośrednikiem w obrocie produktami leczniczymi na terytorium Polski może być tylko podmiot posiadający na terytorium Rzeczypospolitej Polskiej miejsce zamieszkania albo siedzibę i wpisany do Krajowego Rejestru Pośredników w Obrocie Produktami Leczniczymi. Prowadzenie ww. rejestru w systemie teleinformatycznym powierzono Głównemu Inspektorowi Farmaceutycznemu.
W drodze nowelizacji wprowadzono także nowe regulacje dotyczące wysyłkowej sprzedaży produktów leczniczych. W tym zakresie przyjęto m.in. zasadę, że informacje na temat aptek ogólnodostępnych i punktów aptecznych prowadzących wysyłkową sprzedaż produktów leczniczych są gromadzone w Krajowym Rejestrze Zezwoleń na Prowadzenie Aptek Ogólnodostępnych, Punktów Aptecznych oraz Rejestrze Udzielonych Zgód na Prowadzenie Aptek Szpitalnych i Zakładowych. Informacje ujawniane w ww. rejestrach mają być przy tym udostępniane publicznie za pomocą systemu teleinformatycznego.
Jednocześnie na podmioty prowadzące wysyłkową sprzedaż produktów leczniczych nałożono obowiązek zgłaszania do właściwego miejscowo wojewódzkiego inspektora farmaceutycznego informacji podlegających ujawnieniu we wskazanych rejestrach, nie później niż na 14 dni przed planowanym rozpoczęciem prowadzenia tego rodzaju działalności, a następnie niezwłocznego zgłaszania ewentualnych zmian w zakresie ww. informacji. Istotną zmianą jest także rozszerzenie katalogu okoliczności, z uwagi na które wojewódzki inspektor farmaceutyczny cofa zezwolenie na prowadzenie apteki ogólnodostępnej. Wśród ww. okoliczności znalazło się bowiem m.in. prowadzenie przez aptekę sprzedaży wysyłkowej produktów leczniczych wydawanych bez przepisu lekarza bez dokonania zgłoszenia.
Przydatne linki:
- Ustawa z dnia 19 grudnia 2014 r. o zmianie ustawy – Prawo farmaceutyczne oraz niektórych innych ustaw
Zmiany przyjęte nowelizacją objęły także kwestie związane z prowadzeniem hurtowni farmaceutycznych oraz hurtowni farmaceutycznych produktów leczniczych weterynaryjnych. Odnośnie tych zagadnień zmodyfikowano m.in. zakres informacji, które należy podawać we wniosku o udzielenie zezwolenia na prowadzenie ww. hurtowni, a także wyliczenie dokumentów podlegających dołączeniu do takiego wniosku. Co szczególnie istotne z praktycznego punktu widzenia, nowelizacja określiła maksymalny termin, w którym należy rozpatrzyć ww. wniosek, wynoszący 90 dni od dnia złożenia wniosku.
Kolejna ze zmian polega na wprowadzeniu instytucji certyfikatu Dobrej Praktyki Dystrybucyjnej, potwierdzającego zgodność warunków dystrybucji z wymaganiami ww. praktyki. Jak wskazano przy tym w nowelizacji, o przeprowadzenie inspekcji w celu wydania ww. certyfikatu importer lub dystrybutor substancji czynnej może wystąpić do Głównego Inspektora Farmaceutycznego.
Podsumowując, nowelizacja wprowadziła wiele doniosłych zmian w zakresie prawa farmaceutycznego podyktowanych koniecznością dostosowania polskich regulacji do przepisów Unii Europejskiej. Do najistotniejszych z nich należą m.in. nowe przepisy dotyczące sfałszowanego produktu leczniczego, zmiany w zakresie wytwarzania, importu, dystrybucji hurtowej oraz sprzedaży wysyłkowej produktów leczniczych, a także zmiany odnośnie wytwarzania, importu i dystrybucji substancji czynnych. Jak zakłada przy tym ustawodawca, nowe rozwiązania maja zapewnić skuteczniejszy nadzór nad wytwarzaniem i obrotem produktami leczniczymi, a dzięki temu zmniejszyć zagrożenie przenikania do legalnego łańcucha obrotu sfałszowanych produktów leczniczych. Wypada wobec tego mieć nadzieję, że wprowadzone zmiany sprawdzą się w praktyce i przyczynią się do osiągnięcia zamierzonego rezultatu.
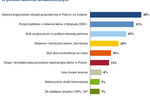
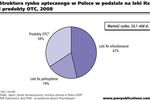
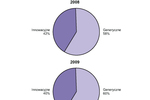 Rynek farmaceutyczny zdominowany przez generyki
Rynek farmaceutyczny zdominowany przez generyki
Przeczytaj także
-
![Rejestracja leków: konieczna integracja [© Syda Productions - Fotolia.com] Rejestracja leków: konieczna integracja]()
Rejestracja leków: konieczna integracja
-
![Znikną apteki internetowe? [© FotoDruk.pl - Fotolia.com] Znikną apteki internetowe?]()
Znikną apteki internetowe?
-
![Prawo farmaceutyczne: monitorowanie działań niepożądanych leków [© Kadmy - Fotolia.com] Prawo farmaceutyczne: monitorowanie działań niepożądanych leków]()
Prawo farmaceutyczne: monitorowanie działań niepożądanych leków
-
![Ochrona patentowa leków [© Africa Studio - Fotolia.com] Ochrona patentowa leków]()
Ochrona patentowa leków
-
![Rynek farmaceutyczny w Polsce rośnie Rynek farmaceutyczny w Polsce rośnie]()
Rynek farmaceutyczny w Polsce rośnie
-
![Rynek farmaceutyczny w Polsce 2009 Rynek farmaceutyczny w Polsce 2009]()
Rynek farmaceutyczny w Polsce 2009
-
![Czy leki biopodobne będą się rozwijać? [© Scanrail - Fotolia.com] Czy leki biopodobne będą się rozwijać?]()
Czy leki biopodobne będą się rozwijać?
-
![Rynek farmaceutyczny w Polsce 2007 Rynek farmaceutyczny w Polsce 2007]()
Rynek farmaceutyczny w Polsce 2007
-
![Polska może być liderem terapii fagowej w UE. Jak wykorzystać szansę? [© pixabay.com] Polska może być liderem terapii fagowej w UE. Jak wykorzystać szansę?]()
Polska może być liderem terapii fagowej w UE. Jak wykorzystać szansę?
Skomentuj artykuł Opcja dostępna dla zalogowanych użytkowników - ZALOGUJ SIĘ / ZAREJESTRUJ SIĘ
Komentarze (0)







![Rejestracja leków: konieczna integracja [© Syda Productions - Fotolia.com] Rejestracja leków: konieczna integracja](https://s3.egospodarka.pl/grafika/rejestracja-lekow/Rejestracja-lekow-konieczna-integracja-d8i3B3.jpg)
![Znikną apteki internetowe? [© FotoDruk.pl - Fotolia.com] Znikną apteki internetowe?](https://s3.egospodarka.pl/grafika2/leki/Znikna-apteki-internetowe-145526-150x100crop.jpg)
![Prawo farmaceutyczne: monitorowanie działań niepożądanych leków [© Kadmy - Fotolia.com] Prawo farmaceutyczne: monitorowanie działań niepożądanych leków](https://s3.egospodarka.pl/grafika2/leki/Prawo-farmaceutyczne-monitorowanie-dzialan-niepozadanych-lekow-126871-150x100crop.jpg)
![Ochrona patentowa leków [© Africa Studio - Fotolia.com] Ochrona patentowa leków](https://s3.egospodarka.pl/grafika2/leki/Ochrona-patentowa-lekow-116995-150x100crop.jpg)
![Czy leki biopodobne będą się rozwijać? [© Scanrail - Fotolia.com] Czy leki biopodobne będą się rozwijać?](https://s3.egospodarka.pl/grafika/leki-biopodobne/Czy-leki-biopodobne-beda-sie-rozwijac-apURW9.jpg)

![Polska może być liderem terapii fagowej w UE. Jak wykorzystać szansę? [© pixabay.com] Polska może być liderem terapii fagowej w UE. Jak wykorzystać szansę?](https://s3.egospodarka.pl/grafika2/bakteriofagi/Polska-moze-byc-liderem-terapii-fagowej-w-UE-Jak-wykorzystac-szanse-256339-150x100crop.jpg)
![E-mail marketing: jak to robić zgodnie z prawem? [© Mathias Rosenthal - Fotolia.com] E-mail marketing: jak to robić zgodnie z prawem?](https://s3.egospodarka.pl/grafika2/e-mail/E-mail-marketing-jak-to-robic-zgodnie-z-prawem-152982-150x100crop.jpg)
![Dobra umowa outsourcingowa, czyli jaka? [© Saklakova - Fotolia.com] Dobra umowa outsourcingowa, czyli jaka?](https://s3.egospodarka.pl/grafika2/uslugi-biznesowe/Dobra-umowa-outsourcingowa-czyli-jaka-153096-150x100crop.jpg)
![Jak odzyskać należności od kontrahenta z Wielkiej Brytanii? [© Depositphotos] Jak odzyskać należności od kontrahenta z Wielkiej Brytanii?](https://s3.egospodarka.pl/grafika2/odzyskiwanie-naleznosci/Jak-odzyskac-naleznosci-od-kontrahenta-z-Wielkiej-Brytanii-259339-150x100crop.jpg)

![Nowe stawki celne w Wielkiej Brytanii szansą dla eksporterów z Polski? [© Elias z Pixabay] Nowe stawki celne w Wielkiej Brytanii szansą dla eksporterów z Polski?](https://s3.egospodarka.pl/grafika2/Wielka-Brytania/Nowe-stawki-celne-w-Wielkiej-Brytanii-szansa-dla-eksporterow-z-Polski-259271-150x100crop.jpg)
![Zwolnienia grupowe: pracownicy muszą pamiętać o swoich prawach [© Andrey Popov - Fotolia.com] Zwolnienia grupowe: pracownicy muszą pamiętać o swoich prawach](https://s3.egospodarka.pl/grafika2/zwolnienia-grupowe/Zwolnienia-grupowe-pracownicy-musza-pamietac-o-swoich-prawach-259265-150x100crop.jpg)
![Ranking kont firmowych 2023. W jakim banku najlepsze konto firmowe? [© Karolina Chaberek - Fotolia.com] Ranking kont firmowych 2023. W jakim banku najlepsze konto firmowe?](https://s3.egospodarka.pl/grafika2/konto-bankowe/Ranking-kont-firmowych-2023-W-jakim-banku-najlepsze-konto-firmowe-251614-150x100crop.jpg)
![Jak pisać i publikować artykuły sponsorowane. 6 najczęściej popełnianych błędów [© nikolai sorokin - fotolia.com] Jak pisać i publikować artykuły sponsorowane. 6 najczęściej popełnianych błędów](https://s3.egospodarka.pl/grafika2/artykul-sponsorowany/Jak-pisac-i-publikowac-artykuly-sponsorowane-6-najczesciej-popelnianych-bledow-228344-150x100crop.jpg)
![Reklama natywna - 5 najważniejszych zalet [© tashatuvango - Fotolia.com] Reklama natywna - 5 najważniejszych zalet](https://s3.egospodarka.pl/grafika2/artykul-natywny/Reklama-natywna-5-najwazniejszych-zalet-226496-150x100crop.jpg)
![Punkty karne 2023. Sprawdź taryfikator [© pixabay.com] Punkty karne 2023. Sprawdź taryfikator](https://s3.egospodarka.pl/grafika2/punkty-karne/Punkty-karne-2023-Sprawdz-taryfikator-249808-150x100crop.jpg)
 ROBYG z nowym etapem Portu Popowice we Wrocławiu
ROBYG z nowym etapem Portu Popowice we Wrocławiu






![Licznik Elektromobilności: 560 nowych punktów ładowania w I kw. 2024 [© Eveline de Bruin z Pixabay] Licznik Elektromobilności: 560 nowych punktów ładowania w I kw. 2024](https://s3.egospodarka.pl/grafika2/motoryzacja/Licznik-Elektromobilnosci-560-nowych-punktow-ladowania-w-I-kw-2024-259370-150x100crop.jpg)

![Marki własne: ciągle za drogie, aby zdobyć rynek? [© sese2018 z Pixabay] Marki własne: ciągle za drogie, aby zdobyć rynek?](https://s3.egospodarka.pl/grafika2/zachowania-konsumentow/Marki-wlasne-ciagle-za-drogie-aby-zdobyc-rynek-259367-150x100crop.jpg)